Det er litt over 10 år siden ruksolitinib ble det første legemidlet godkjent for behandling av myelofibrose. Hvilken betydning har det hatt for vår forståelse av – og tilnærming til – sykdommen?
Myelofibrose (MF) er en type kronisk myeloproliferativ blodkreft som fører til alvorlige komplikasjoner som forstørret milt, unormale cytokinuttrykk, cytopenier og progressiv fibrose i benmargen. Disse fysiologiske forstyrrelsene medfører betydelige symptomer med nedgang i livskvaliteten1 og redusert overlevelse.2 MF er kjent for å være assosiert med dysregulering av JAK1- og JAK2-signalering.3
Første målrettede behandling
Før introduksjonen av ruksolitinib var behandlingsalternativene for MF begrenset til ikke-målrettede behandlinger som hydroksyurea (HU), glukokortikoider og i sjeldnere tilfeller (5–10 %) stamcelletransplantasjon.4
Jakavi™ (ruksolitinib) er på sin side en selektiv hemmer av enzymene JAK1 og JAK2, som medierer signaleringen av en rekke cytokiner og vekstfaktorer viktige for hematopoiese og immunfunksjon.3
Ruksolitinib har flere godt beskrevne bivirkninger, som inkluderer lavere blodverdier, økt mottakelighet for infeksjoner som varicella zoster, og for ikke-melanom hudkreft. Pasienter kan også gå opp i vekt, få økt blodtrykk og forhøyede kolesterolnivåer. Ingen nye bivirkningssignaler har blitt rapportert de siste 5 årene.
Redusert miltstørrelse
De to randomiserte studiene COMFORT-I og COMFORT-II lå til grunn for godkjenning av ruksolitinib for behandling av MF.4 COMFORT-I viste at andelen pasienter som nådde minst en 35 % reduksjon i miltvolum ved uke 24, var 41,9 % for ruksolitinib mot 0,7 % i placebogruppen.5
COMFORT-II fant at 28 % av MF-pasientene som mottok ruksolitinib hadde nådd det primære endepunktet (35 % reduksjon i miltvolum) ved uke 48, mot 0 % som mottok beste tilgjengelige terapi (som var legens foretrukne valg blant tilgjengelige legemidler i Europa).6 I begge studiene ble MF-assosierte symptomer redusert hos de fleste pasientene som mottok ruksolitinib, mens de ble forverret hos majoriteten av pasientene som mottok placebo eller beste tilgjengelige terapi.5,6
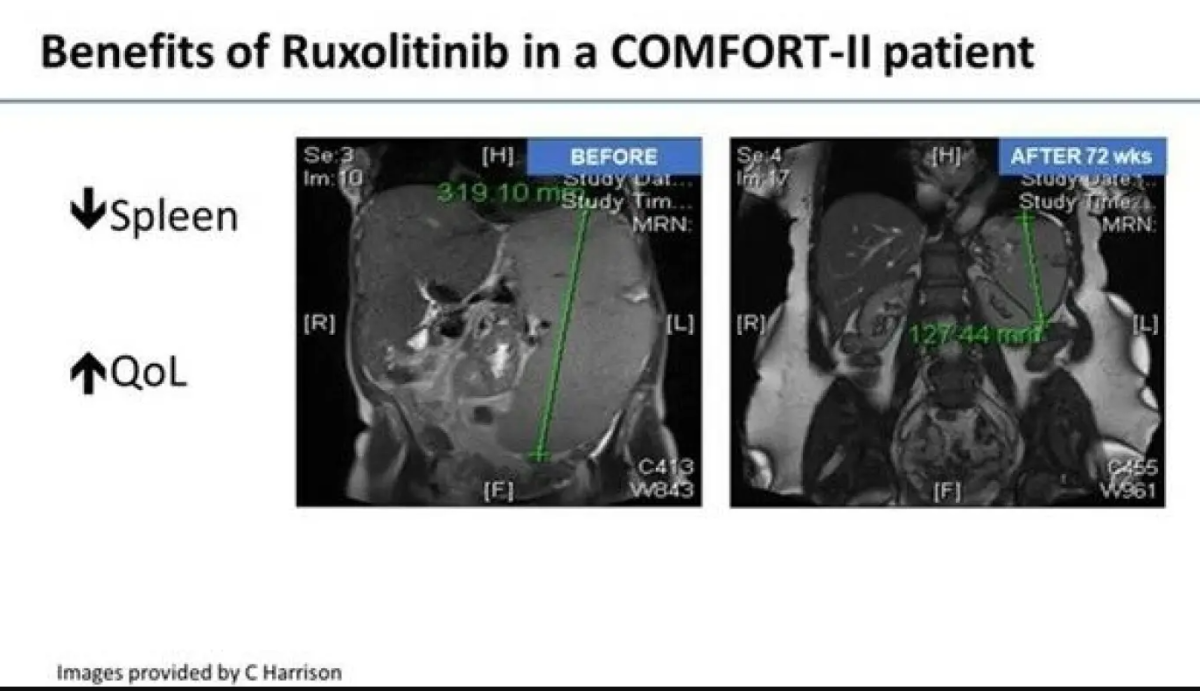
Bildet viser kun én responder. Behandlingsrespons varierer mellom pasienter, og effekten er ikke nødvendigvis overførbar til alle kliniske tilfeller.
Hva har vi lært siden den gangen? 5-årsanalyser av de to studiene har vist at ruksolitinib er forbundet med langvarig reduksjon i miltstørrelse, hvor medianvarigheten på >35 %-reduksjonen var ~3,2 år (med vedlikeholdsterapi) i begge studiene.7,8
– En poolet analyse av disse studiene fant at reduksjon i miltvolum ved uke 24 var korrelert med bedre overlevelse (OS), og at større miltvolum ved baseline korrelerte med verre overlevelse9, sier Claire Harrison, professor i hematologi ved Guy’s and St. Thomas’ Hospital i London.
Økt overlevelse
I løpet av de siste ti årene har vi fått stadig mer data om nettopp overlevelse ved bruk av ruksolitinib for behandling av MF. Allerede i COMFORT I-studien så vi en betydelig bedre overlevelsesrate i ruksolitinib-gruppen5. Det samme fant man også i en femårsanalyse, selv med mulighet for crossover fra placebo-gruppen.7
I en annen samlet femårsanalyse av COMFORT-studiene ble det funnet en 30 % reduksjon i risiko for død i ruksolitinib-gruppen sammenlignet med placebo – uten å ha korrigert for crossover.10
– En nyere poolet analyse på tvers av COMFORT-studiene antyder størst fordel dersom man begynner behandling innen 12 måneder etter diagnose, sier Harrison.11
Også real-world-data viser økt overlevelse blant MF-pasienter behandlet med ruksolitinib.12 Med oppdaterte data fra ERNEST-registeret kunne en studie fra 2022 vise signifikant bedre forlenget median overlevelse med ruksolitinib versus hydroksyurea (6,7 vs. 5,1 år; p < 0.001).13
Bivirkninger ved myelofibrose
Bivirkningene som ble rapportert hyppigst var trombocytopeni og anemi. De tre ikke-hematologiske bivirkningene som var hyppigst rapportert var blåmerker (33,3 %), annen blødning (inkludert neseblødning, postoperativ blødning og hematuri) (24,3 %) og svimmelhet (21,9 %).3
Flere indikasjoner
Myelofibrose er imidlertid ikke den eneste indikasjonen ruksolitinib har. Ruksolitinib er også indisert til behandling av voksne pasienter med polycytemia vera som er resistente mot eller intolerante overfor hydroksyurea.3
PV er en type sjelden blodkreft i samme gruppe som MF, kjennetegnet ved overproduksjon av røde blodceller. Dette fører til tykkere blod, som øker risikoen for trombose, og pasienter har opptil 19 % risiko for å over tid utvikle myelofibrose.14 Pasienter med PV som har høy risiko for trombose, trenger livslang behandling.15
– Hydroksyurea (HU) er den vanligste behandlingen for disse pasientene, men over tid vil 20–25 % slutte å respondere eller utvikle intoleranse for HU. Denne non-responderende pasientgruppen, særlig i kombinasjon med lavere blodverdier, har økt risiko for død, sier professoren.16
En ekspertgruppe nedsatt av European Leukemia Net (ELN) har kommet med et forslag til kriterier for resistens eller intoleranse til HU17, som også Helsedirektoratet henviser til i sine retningslinjer.18 Med disse responskriteriene kan man tidlig identifisere pasienter som responderer dårlig på HU.
Noen PV-resultater
En randomisert, åpen, aktivt kontrollert fase 3-studie (RESPONSE) ble utført hos 222 pasienter som var resistente eller intolerante overfor HU etter disse kriteriene. Det primære kombinerte endepunktet var andelen pasienter som ikke hadde behov for flebotomi (HCT-kontroll) og i tillegg oppnådde en > 35 % reduksjon i miltstørrelse fra baseline ved uke 32.19
Dette ble nådd hos 23 % av pasientene i Jakavi® (ruksolitinib)-gruppen mot 0,8 % som mottok beste tilgjengelige behandling (BTB).18 Hematokrit-kontroll ble oppnådd hos 60 % av pasientene i Jakavi-armen sammenlignet med 18,8 % i BTB-armen. > 35 % reduksjon i miltstørrelse ble oppnådd hos 40 % av pasientene i Jakavi-armen mot 0,9 % i BTB-armen.19
Andelen pasienter som oppnådde kontroll på blodverdiene (CR) var 23,6 % for Jakavi, mens tallet var 8 % for BTB.19
Også fase 2-studien MAJIC-PV fra 2023 sammenlignet ruksolitinib med BTB hos pasienter (n=180) som var resistente/intolerante mot hydroksykarbamid og fulgte pasienter for opptil 5 år. Resultatene viste at det primære utfallet (CR innen 1 år) ble nådd av 43 prosent av pasientene i ruksolitinib-gruppen mot 26 prosent i BTB-armen (p=0,02).20
Hendelsesfri overlevelse (EFS) var bedre både for ruksolitinib-behandlede pasienter (HR: 0,58; p=0,03) og de som oppnådde CR innen 12 måneder (HR: 0,41; p=0,01), og demonstrerte slik fordelen av ruksolitinib, men også viktigheten av CR som mål.20
I alle disse studiene forbedret ruksolitinib også symptomene som kan negativt påvirke PV-pasienters livskvalitet, og MAJIC-PV-studien viste at denne forbedringen varte i nesten et år.19,20
Bivirkninger ved polycytemia vera
De hyppigst rapporterte bivirkningene var anemi og økt alaninaminotransferase. De tre hyppigste ikke-hematologiske bivirkningene var vektøkning (20,3 %), svimmelhet (19,4 %) og hodepine (17,9 %).3
Oppsummering
– Oppsummert viser disse studiene at ruksolitinib representerer et viktig behandlingsalternativ for høyrisiko PV-pasienter som er resistente til hydroksyurea, avslutter Harrison.
Hvorvidt ruksolitinib vil være et like stort steg fremover for PV som det har vært for MF, vil tiden vise. Men noe data fra MAJIC-PV-studien tyder på at legemiddelet forbedrer den molekylære responsen og kan endre antall sykdomsbærende stamceller.20
Sikkerhetsinformasjon
Indikasjon: Jakavi er indisert til behandling av sykdomsrelatert splenomegali eller symptomer hos voksne pasienter med primær myelofibrose (også kjent som kronisk idiopatisk myelofibrose), post-polycytemia vera myelofibrose eller post-essensiell trombocytemi myelofibrose. Jakavi er indisert til behandling av voksne pasienter med polycytemia vera (PV) som er resistente mot eller intolerante overfor hydroksyurea. Jakavi er indisert til behandling av pasienter som er 12 år og eldre med akutt transplantat-mot-vert-sykdom (graft versus host disease, GvHD) eller kronisk transplantat-mot-vert-sykdom (GvHD) som har respondert utilstrekkelig på kortikosteroider eller andre systemiske behandlinger. Dosering: Fullstendig blodcelletelling, inkludert differensialtelling av hvite blodceller, må utføres før behandling med Jakavi startes opp og bør kontrolleres hver 2. til 4. uke til dosering av Jakavi er stabilisert, og deretter etter klinisk behov. Den anbefalte startdosen med Jakavi ved myelofibrose (MF) er basert på blodplatetall. Ved blodplatetall 50 x 109/liter til <75 x 109/liter gis 5 mg oralt to ganger daglig. Ved blodplatetall 75 x 109/liter til <100 x 109/liter gis 10 mg oralt to ganger daglig. Ved blodplatetall 100 til 200 x 109/liter gis 15 mg oralt to ganger daglig. Ved blodplatetall > 200 x 109/liter gis 20 mg oralt to ganger daglig. Den anbefalte startdosen med Jakavi ved polycytemia vera (PV) er 10 mg gitt oralt to ganger daglig. Den anbefalte startdosen med Jakavi ved akutt og kronisk transplantat-mot-vert-sykdom (GvHD) er 10 mg gitt oralt to ganger daglig. Jakavi kan gis samtidig ved fortsatt bruk av kortikosteroider og/eller kalsineurinhemmere. Vanligste bivirkninger: Bivirkninger som ble rapportert for alle indikasjoner var trombocytopeni, anemi, nøytropeni, cytomegalovirus (CMV)- infeksjon, sepsis, blåmerker og blødninger, hyperkolesterolemi, økt alaninamino- og aspartataminotransferase, hodepine og hypertensjon. Kontraindikasjoner: Graviditet og amming. Overfølsomhet overfor virkestoffet eller overfor noen av hjelpestoffene. Advarsler og forsiktighetsregler: Behandling med Jakavi kan føre til hematologiske bivirkninger, inkludert trombocytopeni, anemi og nøytropeni. Risikoen for alvorlige bakterielle og mykobakterielle infeksjoner og sopp- og virusinfeksjoner, bør vurderes. Pasienten bør følges nøye for tegn/symptomer på infeksjoner og egnet behandling initieres straks. Behandling med Jakavi bør ikke startes før aktive, alvorlige infeksjoner er behandlet. Progressiv multifokal leukoencefalopati (PML) er rapportert ved behandling med Jakavi. Pasienter bør monitoreres og ved nyoppståtte eller forverrede symptomer på PML bør pasienten henvises til nevrolog og videre dosering stoppes inntil PML er utelukket. Anbefalt startdose for MF basert på antall blodplater ved enhver form for nedsatt leverfunksjon bør reduseres med ca. 50%, og administrering bør skje 2 ganger daglig. Ved PV er anbefalt startdose 5 mg 2 × daglig ved nedsatt leverfunksjon. Hos pasienter med GvHD og lett, moderat eller alvorlig nedsatt leverfunksjon som ikke er relatert til GvHD, bør startdosen av ruksolitinib reduseres med 50 %. Hos pasienter som har leverrelatert GvHD og en økning av total bilirubin til > 3 x ULN, bør blodtellinger overvåkes oftere for toksisitet, og en dosereduksjon med ett dosenivå er anbefalt. Startdosen ved alvorlig nedsatt nyrefunksjon bør være redusert til ca. 50% og gis 2 ganger daglig ved MF, og 5 mg 2 ganger daglig ved PV og GvHD. Reseptgruppe, refusjon & pris: Reseptgruppe C. Godkjent etter H-resept. Jakavi 20 mg tabletter, 56 stk, kr 42 601,40. Jakavi 15 mg tabletter, 56 stk, kr 42 601,40. Jakavi 10 mg tabletter, 56 stk, kr 42 329,60. Jakavi 5 mg tabletter, 56 stk, kr 21 540,70 per 23.09.2022.
Se Felleskatalogen for mer informasjon: https://www.felleskatalogen.no/medisin/jakavi-novartis-578770

